
全球首款阿尔茨海默药将获FDA审批上市!
“令人震惊”(shocking),“惊人的逆转”(stunning reversal)…这些是美国媒体对渤健(Biogen)公司爆出重磅新闻的描述! 10月23日,美国生物技术公司渤健(Biogen)与其日本合作伙伴卫材(Eisai)宣布,将向美国食品药品管理局(FDA)申请早期阿兹海默症治疗药物“aducanumab”的上市许可(根据与FDA的讨论,渤健公司计划在2020年初提交《生物制剂许可证》申请(BLA).Based on discussions with the FDA, the Company plans to file
a Biologics License Application (BLA) in early 2020.)。

渤健公司表示,经过临床试验和数据分析,该药物对治疗阿兹海默综合症有效。另据路透社报道,渤健公司称,“aducanumab”降低了早期阿尔茨海默患者的临床衰退。接受药物治疗的患者“在认知功能,如记忆力、定向能力和语言能力等方面,都得到了显著的改善,患者还将从日常生活活动中受益,包括进行个人理财,执行家务(例如打扫卫生,购物和洗衣服)以及独立出门旅行。如果获得批准,阿杜卡奴单抗将成为减少阿尔茨海默氏病临床下降的首个疗法,也将成为证明去除淀粉样蛋白β可以带来更好的临床结果的首个疗法。”因此,他们决定向FDA申请药物上市许可,并将继续与包括欧洲和日本在内的国际市场的监管机构进行对话。
阿尔茨海默症俗称老年痴呆症,是一种起病隐匿的进行性发展的神经系统退行性疾病。“由于这种毁灭性疾病影响了全世界数以千万计,今天的宣布在与阿尔茨海默氏症的斗争中确实令人振奋。这是突破性研究的结果,也证明了Biogen坚定不移地遵循科学并为患者做正确的事的决心,” Biogen首席执行官Michel Vounatsos说。 “我们希望为患者提供第一个减少阿尔茨海默氏病临床衰退的疗法的前景,以及这些结果对于针对淀粉样蛋白β的类似方法的潜在影响。”
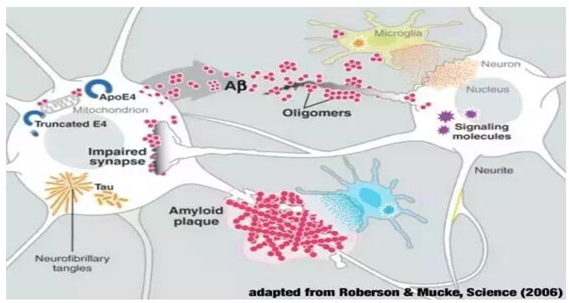
阿尔茨海默病由德国科学家Alois Alzheimer博士最先描述并最先发现,因而国际上便把该病命名为阿尔茨海默病。他描述了这种疾病的两个标志-阿尔茨海默病患者大脑中的斑块和缠结。这些斑块主要保留淀粉样蛋白β(Aβ)肽。淀粉样蛋白β同种型在正常细胞代谢期间由来自淀粉样蛋白前体蛋白(APP)的β-和γ-分泌酶产生并分泌到CSF中(参见[1]和其中的参考文献)。APP是一种完整的膜蛋白,含有695,751或770个氨基酸。已经显示存在许多不同的Aβ同种型。1995年,在老年斑中发现了不同淀粉样蛋白-β肽Aβ(N3pE)的显性和差异沉积[2]。然而,斑块中最丰富的物种是β淀粉样蛋白(1-42),与CSF中年龄匹配的对照组相比,其在AD患者中降低至约50%。
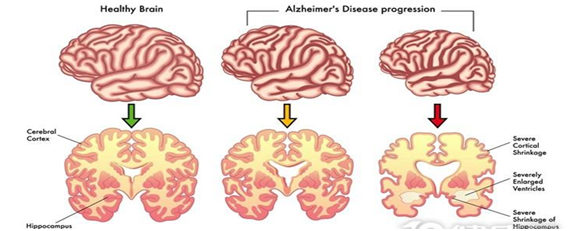
如美国国家老龄化研究所工作组所定义的:阿尔茨海默病的发展具有三个阶段。阿尔茨海默病的临床前阶段,AD导致的轻度认知障碍(MCI)阶段,以及AD导致的痴呆阶段。淀粉样变性早在临床前阶段就会发生。第一个认知缺陷可以在MCI阶段表现出来,而在痴呆阶段,患者无法做任何工作或日常琐事。
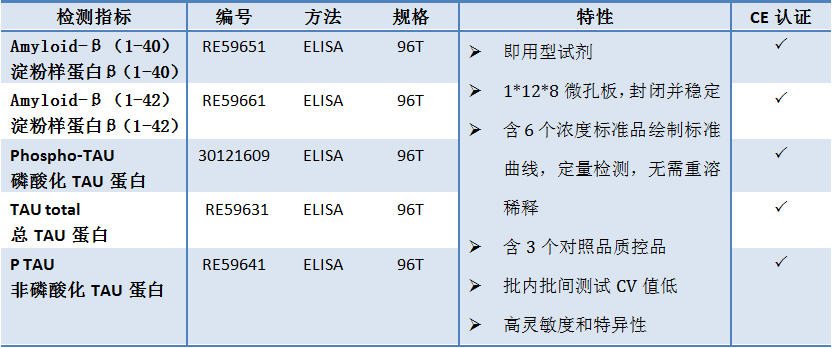
因此,淀粉样蛋白β(1-42)的浓度被认为是诊断阿尔茨海默氏病的有用生物标志物(与其他生物标志物如Tau和Phospho-Tau组合)。此外,许多独立研究(例如[3-5])显示淀粉样蛋白-β(1-42)对淀粉样蛋白-β(1-40)是阿尔茨海默病的优良诊断标志物。
在此领域,IBL International与德国杜伊斯堡-埃森大学(University of Duisburg-Essen, 2018年泰晤士全球年轻大学排名Top20)及IBL Japan合作积极开展阿兹海默症研究资助及基于体液的免疫学检测诊断方法,研制出的高质量诊断级标准(CE认证)试剂盒成功用于临床诊断。深圳科润达生物公司为IBL International国内代理及售后服务商。
在此过程中,我们发现联合检测Aβ42/Aβ40较单独检测Aβ42可以显著提高诊断准确率。脑脊液Aβ42/Aβ40比值测定已作为评价脑Aβ蛋白状态的标准方法。同时,也发现Aβ42/Aβ40与引起神经纤维纠缠的磷酸化Tau(pTau)水平呈良好的相关性。
参考文献:
[1] Blennow K, Zetterberg H, Fagan AM. Fluid biomarkers in Alzheimer disease. Cold Spring Harb PerspectMed 2012;2(9):a006221.
[2] Saido TC, Iwatsubo T, Mann DM, Shimada H, Ihara Y, Kawashima S. Dominant and differentialdeposition of distinct beta-amyloid peptide species,
A beta N3(pE), in senile plaques. Neuron1995;14(2):457–66.
[3] Wiltfang J, Esselmann H, Bibl M, Hull M, Hampel H, Kessler H et al. Amyloid beta peptide ratio 42/40 but not A beta 42 correlates with phospho-Tau in patients with
low- and high-CSF A beta 40 load.J Neurochem 2007;101(4):1053–9.
[4] Kuperstein I, Broersen K, Benilova I, Rozenski J, Jonckheere W, Debulpaep M et al. Neurotoxicity ofAlzheimer's disease Abeta peptides is induced by small
changes in the Abeta42 to Abeta40 ratio.EMBO J 2010;29(19):3408–20.
[5] Spies PE, Slats D, Sjogren JMC, Kremer BPH, Verhey FRJ, Rikkert MGMO et al. The cerebrospinalfluid amyloid beta42/40 ratio in the differentiation of Alzheimer'
s disease from non-Alzheimer'sdementia. Curr Alzheimer Res 2010;7(5):470–6.